|
Le
recueil d’informations lors d’un essai clinique
sur l'Internet consiste ŕ relier un CRF
(Case Report Form - cahier de recueil) électronique ŕ une
base de données. L'interface est réalisée ŕ partir d'un outil
générique (comme en propose par exemple IBM) ou d'une solution
spécifique.
Le
systčme développé par IBM, ClinWare, se compose de plusieurs
applications complémentaires offrant une solution “clé
en main” . Il développe des pages au format HTML et utilise
des applets
Java pour les utilitaires associés aux champs de saisie
(procédure de validation automatique, par exemple) (11).
Le produit se compose de deux
outils :
-
ClinWare
Trial Builder permet d'élaborer un CRF en
fonction de la structure de l'essai et des exigences du
laboratoire. Il possčde également une fonction assurant,
pour certains types de champs, le contrôle automatique
et la validation des données saisies par l'investigateur.
-
ClinWare
Trial Reporter constitue un support pour
créer une base de données reliée au CRF et en assurer
le traitement. Il propose ŕ cette fin une série de notes,
de protocoles et de requętes assurant un audit des CRF.
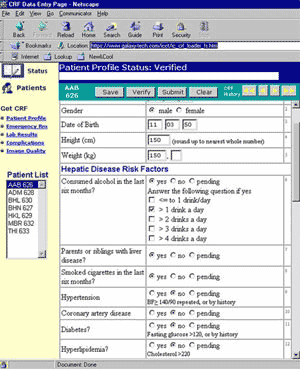
Le
produit proposé par IBM marque le développement d'outils génériques
de gestion informatique des essais. IBM se positionne ici
comme un simple fournisseur de progiciel, affirmant sa volonté
de ne pas empiéter sur les domaines d’action respectifs
des CROs et des laboratoires.
Une
solution générique risque cependant de manquer de souplesse
et de ne pas ętre adaptée ŕ tous les types d'essais. Aussi
performant soit-il, un tel outil peut ne pas offrir toutes
les ressources nécessaires ŕ l'élaboration du CRF (10).
Certains champs ou informations particuličres recquičrent
en effet la création d'outils ad hoc. Par ailleurs, l'ergonomie
du cahier de recueil et la logique de navigation sont déterminants
pour le bon déroulement de l'essai. Or, l'utilisation d'un
outil générique risque de trop encadrer l'architecture du
serveur et peut limiter la liberté des responsables du projet.
La solution qui sera permise par l'utilisation du progiciel
peut ętre moins bien adaptée ŕ l'essai. Certains protocoles
prévoient également que des données soient recueillies directement
par le patient. L'adaptation de progiciels spécifiques et
leur intégration dans l'essai s’avčrent délicates si
le choix du promoteur s'est porté sur un outil générique n'intégrant
pas cette solution. Enfin, au-delŕ de la conception du CRF
électronique et de l'essai clinique lui-męme, l'intégration
au projet de modules de FMC validante ou d'outils d'aide ŕ
la pratique médicale par le laboratoire n'est réalisable qu'avec
des outils spécifiques.
Les
outils génériques ne sont probablement pas adaptés ŕ la totalité
des essais cliniques. La structure du CRF électronique dépend
en effet du type d'essai mené, aussi un outil développé spécifiquement
est-il davantage susceptible de répondre aux exigences de
l'essai et de son protocole (26).
Surtout, l’utilisation d’un outil générique ouvre
la voie ŕ une propriétarisation partielle des solutions (solutions
développées spécifiquement pour l’objet de l’étude).
Copyright © Medcost
2000 -Tous droits réservés.
|
